发布时间:2025-11-27 16:34:57 文章编辑:药队长 推荐人数:
摘要:2025年1月16日,美国食品药品监督管理局正警告医护人员,不要使用由佛罗里达州拉戈市的BPI Labs LLC和宾夕法尼亚州马尔文市的Endo USA生产的未经批准的肾上腺素鼻用溶液。
2025年1月16日
美国食品药品监督管理局正警告医护人员,不要使用由佛罗里达州拉戈市的BPI Labs LLC和宾夕法尼亚州马尔文市的Endo USA生产的未经批准的肾上腺素鼻用溶液。医护人员已将这些产品与FDA批准的静脉注射用肾上腺素产品相混淆。BPI Labs和Endo USA的鼻用溶液绝对不可用于静脉注射。
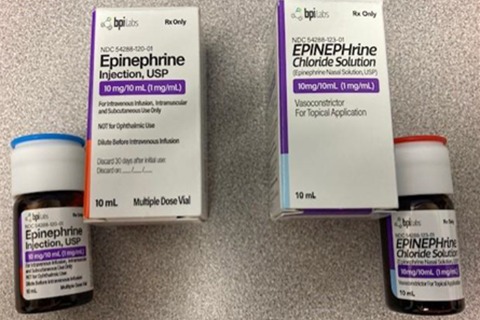
图片来源:drugs
这些鼻用溶液和注射剂产品具有相似的包装和容器,并且由相同的公司生产。鼻用产品与无菌注射剂在瓶子和包装标签上的相似性使得难以区分它们,这可能导致医护人员误将鼻用溶液进行注射,而非使用注射产品。
与注射药物不同,鼻用溶液不要求是无菌的。注射非无菌药物可能导致感染,这对某些患者而言可能危及生命。
医护人员在医院和医疗环境中会使用这两种产品。
2025年12月5日–美国食品药品监督管理局近期查获了数十个单位在诺和诺德授权...【详情】
推荐指数:1182025-12-08
2025年11月21日 自获批以来,美国食品药品监督管理局已收到多例上市后报告,...【详情】
推荐指数:802025-11-28
2025年6月 FDA发布了一份安全通告——《FDA调查非卧床杜氏肌营养不良症患者在...【详情】
推荐指数:792025-11-28
2025年11月10日 美国食品药品监督管理局(FDA)向更年期激素疗法的申请持有人...【详情】
推荐指数:822025-11-28
2025年10月24日 FDA不良事件报告系统(FAERS)收到报告,显示在使用下述特定批...【详情】
推荐指数:802025-11-28
2025年10月21日 FDA正要求修改药品标签,以强化警告:氨甲环酸注射液仅可通过...【详情】
推荐指数:812025-11-27
2025年10月10日 FDA已收到接受Carvykti治疗的患者发生免疫效应细胞相关肠结肠炎...【详情】
推荐指数:812025-11-27
2025年9月25日,美国FDA取消了针对Caprelsa(凡德他尼)的风险评估与缓解策略计...【详情】
推荐指数:802025-11-27
本网站不销售任何药品,只做药品信息资讯展示 网站备案号:京ICP备17022811号-4 药品医疗器械网络信息服务备案:(京)网药械信息备字(2025)第00185号 医药资讯